La chirurgie du rein consiste à retirer la tumeur tout en limitant l’atteinte du tissu rénal sain. La quantité de parenchyme conservée joue un rôle sur la fonction du rein après l’intervention, ce qui influe directement sur l’espérance de vie cancer du rein à long terme. L’association de la reconstruction 3D et de la réalité augmentée s’intègre progressivement à la chirurgie du cancer du rein. Elle permet d’anticiper le geste chirurgical à partir de l’anatomie propre à chaque patient et d’utiliser ces données comme support visuel pendant l’intervention. L’anatomie de chaque patient peut désormais être intégrée au raisonnement opératoire, puis utilisée comme support visuel pendant l’intervention avec un impact direct sur la planification et la précision du geste.
Table des matières:
Qu’est-ce que la réalité augmentée en chirurgie du cancer du rein ?
La réalité augmentée en chirurgie rénale repose sur la superposition d’informations anatomiques virtuelles à l’image réelle transmise par la caméra du robot chirurgical, un outil central de la chirurgie robotique moderne. Le chirurgien observe le rein tel qu’il est exposé au bloc opératoire, enrichi des données issues de l’imagerie préopératoire.
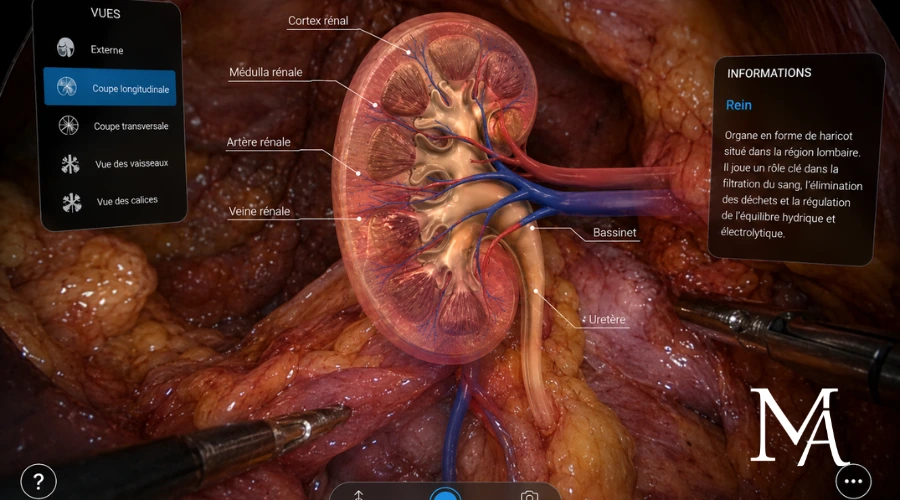
Cette approche apporte un repère supplémentaire dans des situations où l’anatomie est peu lisible, notamment lorsque la tumeur est profonde, partiellement enfouie dans le parenchyme ou située à proximité de structures vasculaires complexes. La réalité augmentée n’automatise pas le geste, elle accompagne la décision et facilite l’anticipation des étapes de l’intervention.
À retenir
La réalité virtuelle permet de visualiser un modèle 3D indépendamment de la vue opératoire. La réalité augmentée, quant à elle, superpose ce modèle à l’image réelle du champ opératoire ce qui modifie directement la navigation pendant l’intervention.
Réalité virtuelle vs réalité augmentée en chirurgie rénale
| Critère | Réalité virtuelle | Réalité augmentée |
|---|---|---|
| Affichage du modèle 3D | Séparé de la vue opératoire | Superposé à l’image peropératoire |
| Impact sur la navigation | Aide à la planification | Modifie la navigation en direct |
| Moment d’utilisation | Avant l’intervention | Pendant l’intervention |
| Lien avec le champ opératoire | Aucune superposition | Superposition en temps réel |
| Ajustement peropératoire | Non applicable | Angle et structures modifiables |
À quoi servent les modèles 3D avant une chirurgie du rein ?
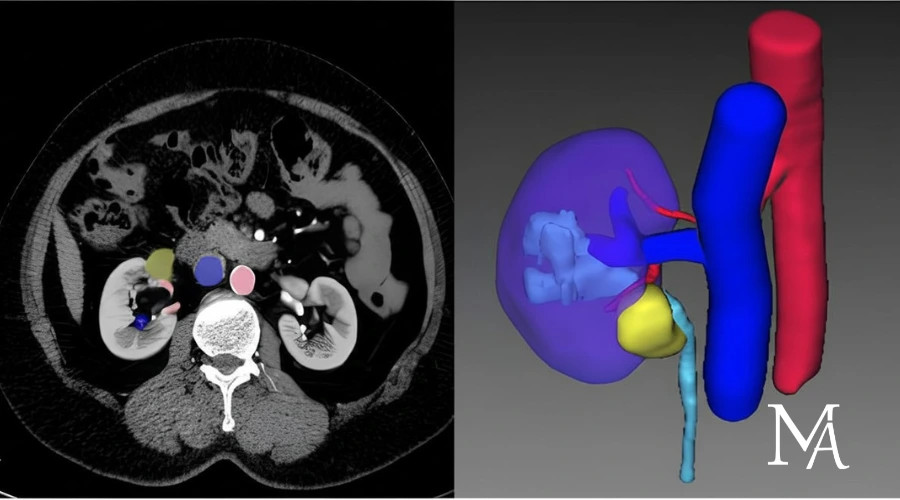
Les modèles 3D sont élaborés à partir d’un scanner injecté réalisé avant l’intervention. Contrairement à une lecture classique en coupes successives, la reconstruction tridimensionnelle restitue une vision globale et cohérente de l’anatomie rénale.
Après une segmentation initiale, le modèle est affiné par des bio-ingénieurs en collaboration avec les radiologues et les chirurgiens urologues. Il intègre les données issues de l’anatomie du rein : volume, tumeur, système collecteur et arbre vasculaire intrarénal. Le chirurgien peut manipuler ce modèle, modifier la transparence des structures, isoler certains vaisseaux ou analyser précisément les rapports entre la tumeur et les zones à risque.
Cette phase de planification permet d’anticiper les difficultés techniques et d’adapter la stratégie opératoire, surtout dans le cadre d’une néphrectomie partielle.
Étapes de la planification 3d et réalité augmentée en chirurgie rénale
| Étape | Action | Acteurs impliqués |
|---|---|---|
| 1 – Imagerie préopératoire | Scanner injecté réalisé avant l’intervention | Radiologue |
| 2 – Segmentation initiale | Reconstruction tridimensionnelle du rein | Bio-ingénieurs |
| 3 – Affinage du modèle | Intégration tumeur, vaisseaux, système collecteur | Bio-ingénieurs / chirurgiens |
| 4 – Analyse de perfusion | Division du rein en territoires vasculaires | Chirurgien / algorithmes |
| 5 – Planification opératoire | Anticipation des difficultés techniques | Chirurgien urologue |
| 6 – Superposition peropératoire | Modèle affiché sur console robotique | Chirurgien urologue |
Comment les modèles 3D aident à préserver le rein pendant l’opération ?
Les modèles 3D ont évolué vers une approche plus fonctionnelle avec le développement des modèles de perfusion vasculaire, décrits dans les travaux relayés par l’European Association of Urology, notamment par Daniele Amparore et Ricardo Autorino.
Ces modèles ne se limitent pas au trajet des artères. Ils analysent les volumes de parenchyme réellement perfusés par chaque branche artérielle. À l’aide d’algorithmes mathématiques, le rein est divisé en territoires de perfusion distincts.
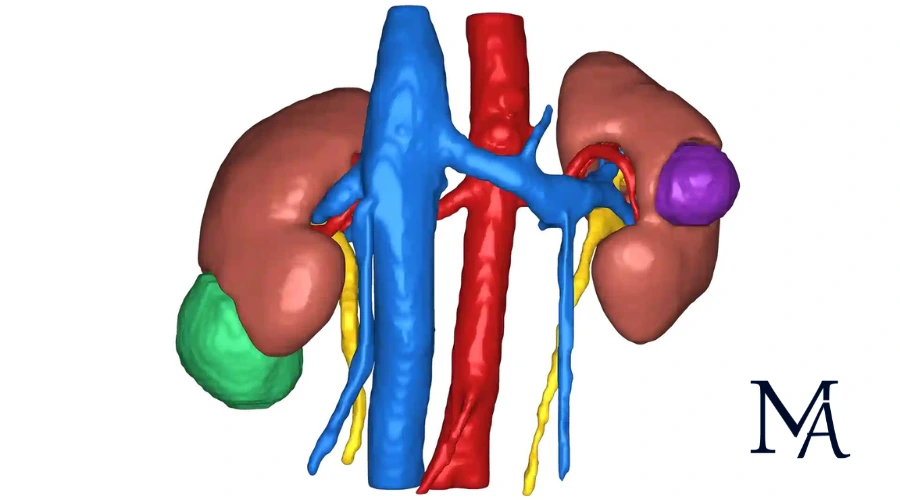
Cette information aide le chirurgien à estimer l’impact d’un clampage sélectif et à limiter l’ischémie au territoire tumoral. Concrètement, elle contribue à préserver davantage de tissu rénal fonctionnel, tout en laissant la possibilité d’ajuster la stratégie en fonction des constatations peropératoires.
À retenir
Les modèles de perfusion vasculaire fournissent une aide à l’analyse. La décision finale repose toujours sur l’anatomie observée pendant l’intervention.
Comment la réalité augmentée guide le chirurgien pendant l’opération ?
Au bloc opératoire, la réalité augmentée accompagne la néphrectomie partielle robot-assistée, une technique utilisant le même robot Da Vinci, à différents moments de l’intervention. Après la phase de planification, le modèle 3D peut être utilisé comme support cognitif ou être superposé directement à la vue endoscopique.
Pour les tumeurs endophytes ou postérieures souvent difficiles à repérer à l’oeil, la superposition virtuelle aide à localiser les limites tumorales et leurs extensions intrarénales. Pour les lésions plus visibles, l’intérêt porte surtout sur l’analyse fine des rapports vasculaires et du système collecteur.
Les images sont affichées sur la console robotique par un dispositif dédié. Le chirurgien peut ajuster le modèle en temps réel en modifiant l’angle de vue ou en masquant certaines structures, ce qui facilite la navigation anatomique pendant la dissection, l’exérèse et la reconstruction.
Apports et limites de la réalité augmentée en néphrectomie partielle
| Dimension | Apport / Avantage | Limite / Point de vigilance |
|---|---|---|
| Repérage tumoral | Localise les tumeurs profondes/endophytes | Surtout utile pour lésions complexes |
| Préservation rénale | Limite l’atteinte du parenchyme sain | Ajustement selon constatations peropératoires |
| Vasculaire | Analyse fine des rapports artériels | Décision finale reste clinique |
| Automatisation | Accompagne la décision du chirurgien | Ne remplace pas le geste chirurgical |
| Généralisation | Technologie en progression active | Indications à préciser à grande échelle |
Quelle place pour la réalité augmentée dans la chirurgie du cancer du rein ?
Les recherches menées en France, notamment au CHU de Bordeaux, montrent bien l’évolution progressive de ces technologies. Des jumeaux numériques du rein sont développés à partir de l’imagerie. Ils sont d’abord utilisés séparément de la vue opératoire puis superposés de manière plus précise grâce à des outils capables d’aligner les structures en temps réel.
Cette méthode répond à une difficulté anatomique bien connue : le rein est un organe profond entouré de graisse dont les repères sont parfois difficiles à identifier pendant l’intervention. Une vision augmentée permet de réduire les incertitudes peropératoires et de mieux préserver les structures indispensables à la fonction rénale.
Dans cette optique, des chirurgiens urologues comme le Pr Messas intègrent ces outils dans leur réflexion opératoire, en lien étroit avec les équipes d’imagerie et d’ingénierie biomédicale.
Questions fréquentes sur l’utilisation de la réalité augmentée dans la chirurgie des cancers rénaux
Comment fonctionne la réalité augmentée en chirurgie du cancer du rein ?
Elle repose sur la superposition d’un modèle 3D issu du scanner préopératoire à l’image réelle du champ opératoire, afin d’enrichir la vision du chirurgien pendant l’intervention.
La réalité augmentée est-elle utilisée pour toutes les tumeurs rénales ?
Elle est surtout indiquée pour les tumeurs complexes, profondes ou proches des structures vasculaires, en particulier dans le cadre d’une chirurgie conservatrice du rein.
Quelle est la différence entre réalité virtuelle et réalité augmentée en chirurgie rénale ?
La réalité virtuelle affiche le modèle 3D séparément de la vue opératoire, alors que la réalité augmentée le superpose directement à l’image peropératoire.
Quels sont les bénéfices de la réalité augmentée pour le patient opéré d’un cancer du rein ?
Elle sert d’aide visuelle au chirurgien pour mieux repérer la tumeur et les structures à préserver pendant l’intervention, faciliter une exérèse plus ciblée et limiter l’atteinte du parenchyme rénal sain, ce qui influence la fonction du rein après l’opération.
La réalité augmentée va-t-elle se généraliser en chirurgie du cancer du rein ?
Son utilisation progresse et des travaux cliniques sont en cours pour préciser ses indications et son intérêt réel à plus grande échelle.
Références bibliographiques
- Hughes-Hallett A, Mayer EK, Marcus HJ et al.. « Augmented reality partial nephrectomy: examining the current status and future perspectives. ». Urology. 2014. 83(2):266-73. PubMed PMID:24149104
- Khaddad A, Bernhard JC, Margue G et al.. « A survey of augmented reality methods to guide minimally invasive partial nephrectomy. ». World J Urol. 2023. 41(2):335-343. PubMed PMID:35776173
- Cheng C, Lu M, Zhang Y et al.. « Effect of augmented reality navigation technology on perioperative safety in partial nephrectomies: A meta-analysis and systematic review. ». Front Surg. 2023. 10:1067275. PubMed PMID:37123539
- Piana A, Amparore D, Sica M et al.. « Automatic 3D Augmented-Reality Robot-Assisted Partial Nephrectomy Using Machine Learning: Our Pioneer Experience. ». Cancers (Basel). 2024. 16(5). PubMed PMID:38473404
- Azhar RA. « The influence of 3D renal reconstruction on surgical planning for complex renal tumors: An interactive case-based survey. ». Int Braz J Urol. 2023. 49(3):372-382. PubMed PMID:37115181

Chirurgien Urologue à Paris
Spécialisé en technique mini-invasives, chirurgie robotique et traitement focal du cancer de prostate










